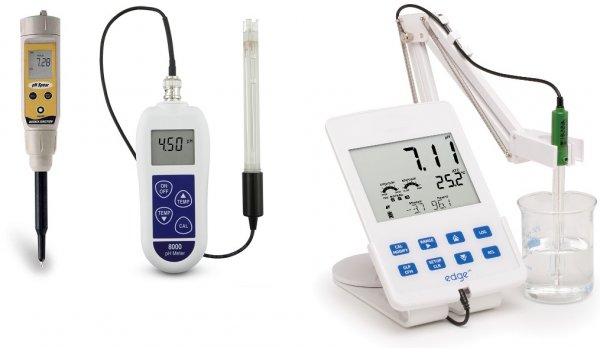
Princip měření pH, zařízení a typy pH metrů
Pro rychlé určení úrovně pH (jinými slovy úrovně kyselosti) různých médií se používají pH metry. Průmyslová nebo pitná voda, roztok kyselin, solí nebo zásad, krev, moč a jiné tělesné tekutiny, ovoce, zelenina a jiné potraviny, léčiva atd. — v zásadě se vše může stát předmětem operačního výzkumu hodnoty pH.
Měření PH je v podstatě měření aktivity vodíkových iontů v médiu. A i samotné označení pH je doslovně přeloženo z latinského „pondus Hydrogenii“ jako „váha vodíku“.
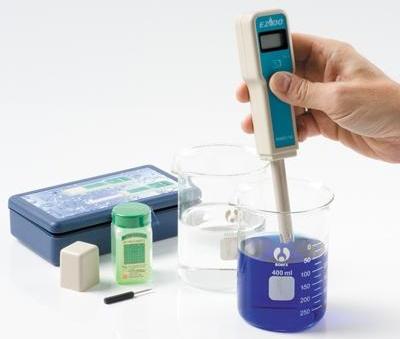
pH metry jsou dnes široce používány v mikrobiologii a medicíně, v úpravě vody a agrochemii, v půdě, v hydroponii, v laboratorním a terénním výzkumu, v chemickém a potravinářském průmyslu, v akvaristice a na mnoha dalších místech.
Moderní pH metr umožňuje přesně a rychle určit hodnotu pH.Pokud je pH 7, je médium neutrální, jako je destilovaná voda, ve které jsou kladné vodíkové ionty H + a záporné hydroxidové ionty OH- rovnoměrně rozděleny. Pokud je kyselost vyšší než 7, pak je médium alkalické. Pokud je pH nižší než 7, médium je kyselé.
A přestože chemici vždy dokázali určit kyselost média klasickou metodou, pomocí indikátorů, například fenolftaleinu, v některých procesech je prostě nutné tento indikátor přesně kvantifikovat a někdy je nutné neustále sledovat to, zařídit to opravit. K tomu byly vynalezeny pH metry.
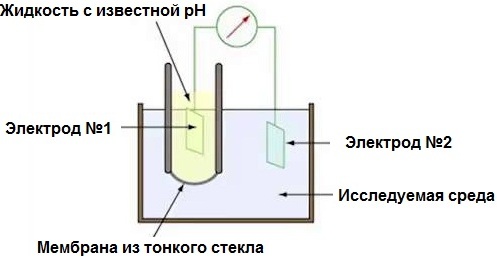
pH metr je ve skutečnosti elektronický milivoltmetr, protože měří potenciálový rozdíl v elektrochemickém systému dvojice elektrod a testovacího média, ve kterém jsou umístěny. Je pravda, že stupnice zařízení je zde odstupňována nikoli v milivoltech, ale v pH, protože naměřené EMF se ukazuje jako úměrné pH.
Dvě elektrody: skleněný indikátor (oxidanty se nebojí borosilikátového skla) a chlorid stříbrný - další referenční elektroda. Skleněná elektroda má velmi vysoký odpor desítek megaohmů, a to je pouze základní požadavek — odpor sondy by neměl být menší než 0,1 GΩ. pH metr je kalibrován pomocí tlumivých roztoků o známém pH.
Vzhledem k tomu, že hodnota EMF je ovlivněna teplotou, má každý takový měřicí přístroj teplotní kompenzaci pro měření při teplotách jiných než + 25 °C.Ale aby bylo dosaženo velmi vysoké přesnosti, je nutné měřit přesně při teplotě + 25 ° C, proto je mnoho pH metrů vybaveno vestavěným teploměrem, takže můžete okamžitě sledovat teplotu média v proces výzkumu.
Skleněná indikační elektroda v podobě trubičky s tenkostěnnou kuličkou na konci, vyrobená ze speciálního elektricky vodivého borosilikátového skla, je v podstatě zapojena do elektrického obvodu. Pohyb kladných iontů H + uvnitř takového skla umožňuje jeho použití (kationty uvnitř skla se pohybují vzhledem k polyaniontu kyseliny křemičité). Do zkumavky se nalije suspenze chloridu stříbrného v roztoku kyseliny chlorovodíkové, načež se do ní ponoří stříbrný drát - tak se získá elektroda chloridu stříbrného.
Skleněná elektroda se spustí do testovacího média, elektrický obvod se uzavře umístěním další referenční elektrody (rtuť-kalomelová pasta v roztoku chloridu draselného) do něj (přes elektrolytický spínač nebo přímo). Chlorid draselný vytváří kontakt mezi rtuť-kalomelovou částí článku a testovacím médiem. Tato přídavná elektroda je obvykle umístěna ve skleněném pouzdře, které je nepropustné pro ionty H +.
Vodivý kontakt roztoku chloridu draselného v referenční elektrodě s testovaným roztokem je tvořen tenkým závitem nebo kapilárou ve skleněném pouzdře.Takto se z referenční elektrody a elektrody chloridu stříbrného získá galvanický článek. elektrolytová část článku obsahuje vodivý skleněný film a testovací prostředí.
EMF elektrodového systému se měří milivoltmetrem, jeho stupnice je odstupňována v pH.Elektrony z elektrody chloridu stříbrného jsou přenášeny na referenční elektrodu působením měřeného EMF, které je vždy doprovázeno přenosem stejného počtu protonů z vnitřku skleněné elektrody do média.
Pokud v tomto případě vezmeme koncentraci kladných vodíkových iontů H + v konstantě skleněné elektrody, pak EMF bude funkcí aktivity H +, tedy funkcí pH studovaného média.
Moderní modely pH metrů fungují díky mikroprocesorům, které provádějí teplotní kompenzaci a řeší mnoho souvisejících úloh. Čím je zařízení složitější, tím více úkolů dokáže vyřešit. Třída přesnosti přístrojů se liší podle modelu a pro různé aplikace lze vybrat vhodný pH metr.
Existují kapesní domácí pH metry, existují profesionální laboratorní, přenosné a průmyslové stacionární. Některé pH metry měří koncentraci iontů v médiu, obsah dusičnanů apod., mají vestavěnou paměť pro uložení výsledků, možnost komunikace s počítačem a funkci úpravy parametrů zpětnovazební smyčkou.