Elektrický proud v kapalinách a plynech
Elektrický proud v kapalinách
 V kovovém vodiči elektřina je tvořen usměrněným pohybem volných elektronů a že nedochází k žádným změnám v látce, z níž je vodič vyroben.
V kovovém vodiči elektřina je tvořen usměrněným pohybem volných elektronů a že nedochází k žádným změnám v látce, z níž je vodič vyroben.
Takové vodiče, u kterých není průchod elektrického proudu doprovázen chemickými změnami v jejich hmotě, se nazývají vodiče první třídy... Patří sem všechny kovy, uhlí a řada dalších látek.
Ale v přírodě existují i takové vodiče elektrického proudu, ve kterých při průchodu proudu dochází k chemickým jevům. Těmto vodičům se říká vodiče druhého druhu... Patří mezi ně především různé roztoky kyselin, solí a zásad ve vodě.
Pokud nalijete vodu do skleněné nádoby a přidáte do ní několik kapek kyseliny sírové (nebo nějaké jiné kyseliny nebo zásady) a poté vezmete dvě kovové desky a připevníte k nim dráty, spustíte tyto desky do nádoby a zapojíte proud zdroj na druhé konce vodičů přes spínač a ampérmetr, pak se plyn z roztoku uvolní a bude to pokračovat nepřetržitě, dokud bude okruh uzavřen.okyselená voda je skutečně vodič. Kromě toho se desky začnou pokrývat bublinami plynu. Poté se tyto bubliny oddělí od talířů a vyjdou ven.
Když roztokem prochází elektrický proud, dochází k chemickým změnám, které mají za následek uvolnění plynu.
Říká se jim vodiče druhého typu elektrolytů a jev, ke kterému v elektrolytu dochází, když jím prochází elektrický proud, je elektrolýza.
Kovové desky ponořené do elektrolytu se nazývají elektrody; jeden z nich připojený ke kladnému pólu zdroje proudu se nazývá anoda a druhý připojený k zápornému pólu je katoda.
Co určuje průchod elektrického proudu v kapalném vodiči? Ukazuje se, že v takových roztocích (elektrolytech) se molekuly kyselin (zásady, sůl) působením rozpouštědla (v tomto případě vody) rozpadají na dvě složky a jedna část molekuly má kladný elektrický náboj a druhá negativní.
Částice molekuly, které mají elektrický náboj, se nazývají ionty... Když se kyselina, sůl nebo zásada rozpustí ve vodě, objeví se v roztoku velké množství kladných i záporných iontů.
Nyní by mělo být jasné, proč roztokem procházel elektrický proud, protože mezi elektrodami připojenými ke zdroji proudu a potenciální rozdíljinými slovy, jeden z nich se ukázal být kladně nabitý a druhý záporně nabitý. Pod vlivem tohoto rozdílu potenciálu se kladné ionty začaly mísit směrem k záporné elektrodě - katodě a záporné ionty - směrem k anodě.
Chaotický pohyb iontů se tak stal uspořádaným opačným pohybem záporných iontů v jednom směru a kladných iontů ve druhém.Tento proces přenosu náboje je tok elektrického proudu elektrolytem a probíhá tak dlouho, dokud existuje potenciálový rozdíl mezi elektrodami. Jakmile rozdíl potenciálů zmizí, proud elektrolytem se zastaví, uspořádaný pohyb iontů se naruší a chaotický pohyb začne znovu.
Jako příklad uvažujme jev elektrolýzy, kdy elektrický proud prochází roztokem síranu měďnatého CuSO4 s měděnými elektrodami spuštěnými do něj.
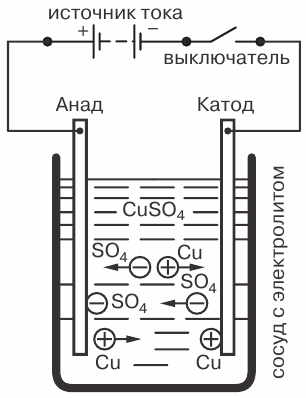
Jev elektrolýzy, kdy proud prochází roztokem síranu měďnatého: C — nádoba s elektrolytem, B — zdroj proudu, C — spínač
Dojde také ke zpětnému pohybu iontů k elektrodám. Kladným iontem bude ion mědi (Cu) a záporným iontem bude zbytek kyseliny (SO4). Ionty mědi se při kontaktu s katodou vybijí (připojí k sobě chybějící elektrony), to znamená, že se přemění na neutrální molekuly čisté mědi a budou se ukládat na katodě ve formě nejtenčí (molekulární ) vrstva.
Záporné ionty, které se dostanou k anodě, jsou také vyvrženy (darují přebytečné elektrony). Zároveň však vstupují do chemické reakce s mědí anody, v důsledku čehož se ke zbytku kyseliny SO4 přidá molekula mědi Cti a vytvoří se molekula síranu měďnatého CnasO4 a vrátí se zpět do elektrolyt.
Protože tento chemický proces trvá dlouho, dochází k usazování mědi na katodě, která se uvolňuje z elektrolytu. V tomto případě elektrolyt místo molekul mědi, které šly na katodu, přijímá nové molekuly mědi v důsledku rozpuštění druhé elektrody, anody.
Stejný proces probíhá, pokud se místo mědi použijí zinkové elektrody a elektrolytem je roztok síranu zinečnatého ZnSO4.Zinek bude také převeden z anody na katodu.
Rozdíl mezi elektrickým proudem v kovech a kapalných vodičích tedy spočívá v tom, že v kovech jsou nosiči náboje pouze volné elektrony, tzn. záporné náboje v elektrolytech elektřina nesené opačně nabitými částicemi hmoty — ionty pohybujícími se v opačných směrech. Proto se říká, že elektrolyty mají iontovou vodivost.

Fenomén elektrolýzy objevil v roce 1837 B. S. Jacobi, který provedl četné experimenty ke studiu a zlepšení chemických zdrojů proudu. Jacobi zjistil, že jedna z elektrod umístěných v roztoku síranu měďnatého, když přes ni procházel elektrický proud, byla potažena mědí.
Tento jev se nazývá elektroformování, nyní nachází extrémně velké praktické uplatnění. Jedním z příkladů je potahování kovových předmětů tenkou vrstvou jiných kovů, například niklování, zlacení, stříbro atd.
Elektrický proud v plynech
Plyny (včetně vzduchu) za normálních podmínek nevedou elektrický proud. Například gól dráty pro venkovní vedeníjsou zavěšeny paralelně k sobě a jsou od sebe izolovány vrstvou vzduchu.
Pod vlivem vysoké teploty, velkého potenciálového rozdílu a dalších důvodů se však plyny, jako kapalné vodiče, ionizují, to znamená, že se v nich ve velkém množství objevují částice molekul plynu, které jako nosiče elektřiny přispívají k průchodu elektrického proudu procházejícího plynem.
Ale zároveň se ionizace plynu liší od ionizace kapalného vodiče.Pokud se molekula v kapalině rozdělí na dvě nabité části, pak se v plynech působením ionizace z každé molekuly vždy oddělí elektrony a iont zůstane ve formě kladně nabité části molekuly.
Stačí zastavit ionizaci plynu, protože přestává být vodivý, zatímco kapalina vždy zůstává vodičem elektrického proudu. Proto je vodivost plynu dočasným jevem, závislým na působení vnějších příčin.

Je tu však ještě něco jiného druh elektrického výbojeNazývá se obloukový výboj nebo jednoduše elektrický oblouk. Fenomén elektrického oblouku objevil na počátku 19. století první ruský elektrotechnik V. V. Petrov.
V.V. Při provádění četných experimentů Petrov zjistil, že mezi dvěma uhlíky připojenými ke zdroji proudu se ve vzduchu objevil nepřetržitý elektrický výboj doprovázený jasným světlem. V. V. Petrov ve svých spisech napsal, že v tomto případě „může být temný klid dostatečně jasně osvětlen“. Tak bylo poprvé získáno elektrické světlo, které prakticky aplikoval další ruský elektroinženýr Pavel Nikolajevič Jabločkov.
"Svesht Yablochkov", jehož práce je založena na použití elektrického oblouku, udělal v té době skutečnou revoluci v elektrotechnice.

Obloukový výboj se dnes používá jako zdroj světla například v reflektorech a promítacích zařízeních. Vysoká teplota obloukového výboje umožňuje jeho použití pro zařízení obloukových pecí… V současné době se obloukové pece poháněné velmi vysokým proudem používají v řadě průmyslových odvětví: pro tavení oceli, litiny, feroslitin, bronzu atd. A v roce 1882 společnost NN Benardos poprvé použila obloukový výboj pro řezání a svařování kovu.
V plynových potrubích, zářivkách, stabilizátorech napětí, k získání elektronových a iontových paprsků, tzv. doutnavého výboje.
Jiskrový výboj Slouží k měření velkých rozdílů potenciálů pomocí kulového jiskřiště, jehož elektrodami jsou dvě kovové kuličky s leštěným povrchem. Kuličky se pohybují od sebe a je na ně aplikován měřitelný rozdíl potenciálu. Kuličky se pak přibližují k sobě, dokud mezi nimi neprojde jiskra. Když znají průměr kuliček, vzdálenost mezi nimi, tlak, teplotu a vlhkost vzduchu, zjistí potenciální rozdíl mezi koulemi podle speciálních tabulek. Touto metodou je možné změřit s přesností několika procent potenciálový rozdíl v řádu desítek tisíc voltů.
